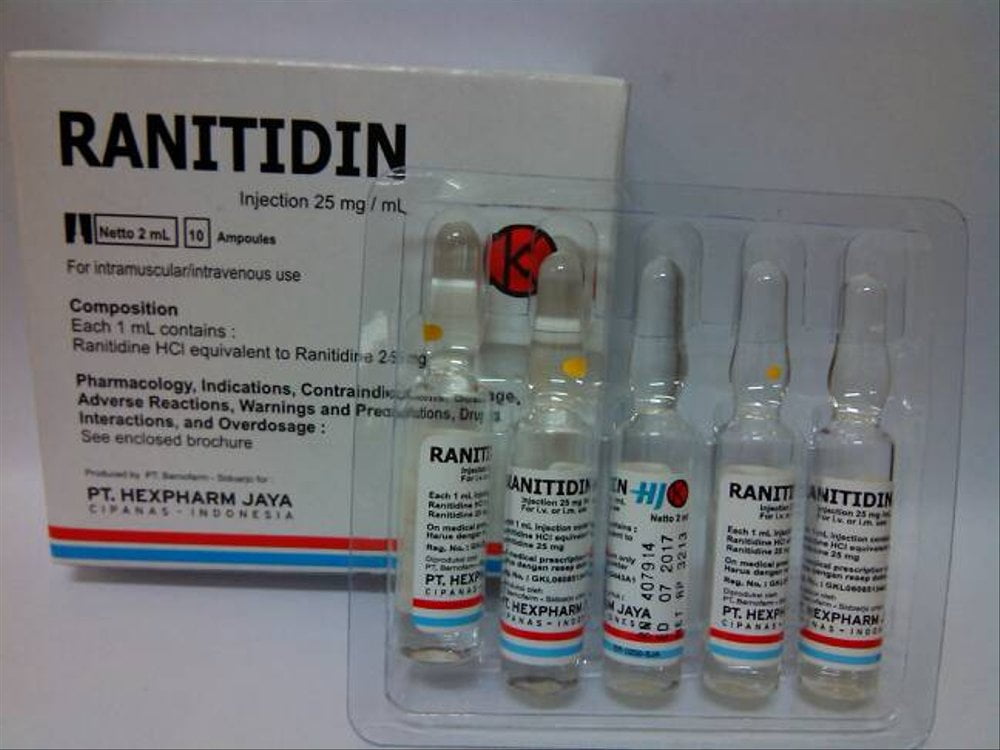
EDITOR.ID, Jakarta,- Badan Pengawas Obat dan Makanan (BPOM) RI memerintahkan penarikan obat lambung ranitidin dari peredaran. Apa alasannya? Pasalnya obat yang mengandung ranitidin berpotensi memicu kanker.
Hasil temuan dan peringatan yang dikeluarkan Badan Kesehatan Amerika (Food and Drug Administration/ US FDA) dan European Medicine Agency (EMA) menyatakan bahwa senyawa ranitidin yang terkontaminasi N-Nitrosodimethylamine (NDMA) dapat memicu kanker.
Ada 5 produk obat lambung yang ditarik BPOM. Produk obat yang ditarik BPOM dilakukan dengan perintah penarikan maupun penarikan sukarela.
Dikutip dari situs resmi situs resmi pom.go.id, berikut penjelasan BPOM terkait ditariknya beberapa produk obat lambung ranitidin.

Ranitidin adalah obat yang digunakan untuk pengobatan gejala penyakit tukak lambung dan tukak usus.
Badan POM telah memberikan persetujuan terhadap ranitidin sejak tahun 1989 melalui kajian evaluasi keamanan, khasiat, dan mutu. Ranitidin tersedia dalam bentuk sediaan tablet, sirup, dan injeksi.
Dalam keterangan tertulis di situs resminya, BPOM menyebut penarikan ini dilakukan karena adanya temuan cemaran NDMA (N-Nitrosodimethylamine) dalam jumlah yang relatif kecil pada sampel produk yang mengandung bahan aktif ranitidin. NDMA merupakan turunan zat Nitrosamin yang dapat terbentuk secara alami.
Meski begitu, studi global memutuskan nilai ambang batas cemaran NDMA yang diperbolehkan adalah 96 ng/hari (acceptable daily intake). NDMA bisa bersifat karsinogenik alias memicu kanker jika dikonsumsi di atas ambang batas secara terus menerus dalam jangka waktu yang lama.
“Dalam rangka kehati-hatian, Badan POM telah menerbitkan Informasi Awal untuk Tenaga Profesional Kesehatan pada tanggal 17 September 2019 terkait Keamanan Produk Ranitidin yang terkontaminasi NDMA,” tulis BPOM, dalam keterangan tertanggal 4 Oktober 2019.
Badan POM saat ini sedang melakukan pengambilan dan pengujian beberapa sampel produk ranitidin. Hasil uji sebagian sampel mengandung cemaran NDMA dengan jumlah yang melebihi batas yang diperbolehkan. Pengujian dan kajian risiko akan dilanjutkan terhadap seluruh produk yang mengandung ranitidin.
“Berdasarkan nilai ambang batas cemaran NDMA yang diperbolehkan, Badan POM memerintahkan kepada Industri Farmasi pemegang izin edar produk tersebut untuk melakukan penghentian produksi dan distribusi serta melakukan penarikan kembali (recall) seluruh bets produk dari peredaran,” sebut BPOM.